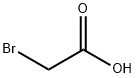
| Kimyoviy xossalari |
OQ dan och sariq ranggacha bo'lgan kristall massa |
| Foydalanadi |
Organik sintez, o'rim-yig'imda tsitrus mevalarining ajralishi. |
| Foydalanadi |
Bromoasetik kislota organik sintezda va alkillashtiruvchi vosita sifatida ishlatiladi. Bundan tashqari, u proteomik tadqiqotlar uchun biokimyoviy sifatida ishlatiladi. Bu muhim xom ashyo va organik sintez, farmatsevtika, bo'yoq va agrokimyoda qo'llaniladigan oraliq mahsulot. |
| Foydalanadi |
Bromoasetik kislota asosan quyidagilar uchun ishlatiladiN-qatron bilan bog'langan peptidlarning terminal bromoatsilatsiyasi.
Bundan tashqari, foydalanish mumkin:sintez qilish (Z)-2-(siklookt-4-en-1-iloksi)sirka kislotasi.
Sintezlash uchun -bromo-fenilasetamid.
Aromatik tiosemikarbazonlarni tiazolilgidrazonlarga aylantirish uchun.
|
| Umumiy tavsif |
Suvli eritma. |
| Havo va suv reaktsiyalari |
Suvda eriydi. |
| Reaktivlik profili |
Karboksilik kislotalar, masalan, BROMOASETIK kislota, agar ularni qabul qilish uchun asos mavjud bo'lsa, vodorod ionlarini beradi. Ular organik (masalan, aminlar) va noorganik barcha asoslar bilan shu tarzda reaksiyaga kirishadilar. Ularning asoslar bilan boʻlgan reaksiyalari “neytrallanishlar” deb ataladigan boʻlsa, katta miqdorda issiqlik evolyutsiyasi bilan kechadi. Kislota va asos o'rtasidagi neytrallanish suv va tuz hosil qiladi. Olti yoki undan kam uglerod atomiga ega bo'lgan karboksilik kislotalar suvda erkin yoki o'rtacha darajada eriydi; oltidan ortiq uglerodga ega bo'lganlar suvda ozgina eriydi. Eriydigan karboksilik kislota suvda vodorod ionlarini hosil qilish uchun ma'lum darajada dissotsilanadi. Shuning uchun karboksilik kislotalar eritmalarining pH qiymati 7 dan kam.0. Ko'pgina erimaydigan karboksilik kislotalar kimyoviy asosga ega bo'lgan suvli eritmalar bilan tez reaksiyaga kirishadi va neytrallanish natijasida eriydigan tuz hosil bo'ladi. Suvli eritmadagi karboksilik kislotalar va suyuq yoki erigan karboksilik kislotalar faol metallar bilan reaksiyaga kirishib, gazsimon vodorod va metall tuzini hosil qilishi mumkin. Bunday reaktsiyalar printsipial jihatdan qattiq karboksilik kislotalar uchun ham sodir bo'ladi, lekin agar qattiq kislota quruq qolsa, sekin kechadi. Hatto "erimaydigan" karboksilik kislotalar ham havodan etarli miqdorda suvni o'zlashtirishi va temir, po'lat va alyuminiy qismlar va idishlarni zanglash yoki eritish uchun Bromoasetik kislotada etarli darajada eriydi. Karboksilik kislotalar, boshqa kislotalar kabi, siyanid tuzlari bilan reaksiyaga kirishib, gazsimon vodorod siyanidini hosil qiladi. Quruq, qattiq karboksilik kislotalar uchun reaksiya sekinroq kechadi. Erimaydigan karboksilik kislotalar siyanidlar eritmalari bilan reaksiyaga kirishib, gazsimon vodorod siyanidini chiqaradi. Yonuvchan va / yoki zaharli gazlar va issiqlik karboksilik kislotalarning diazo birikmalar, ditiokarbamatlar, izosiyanatlar, merkaptanlar, nitridlar va sulfidlar bilan reaksiyaga kirishishi natijasida hosil bo'ladi. Karboksilik kislotalar, ayniqsa suvli eritmalarda, shuningdek, sulfitlar, nitritlar, tiosulfatlar (H2S va SO3 berish uchun), ditionitlar (SO2) bilan reaksiyaga kirishib, yonuvchi va/yoki zaharli gazlar va issiqlik hosil qiladi. Ularning karbonatlar va bikarbonatlar bilan reaktsiyasi zararsiz gaz (karbonat angidrid) hosil qiladi, lekin baribir issiqlik. Boshqa organik birikmalar singari, karboksilik kislotalar ham kuchli oksidlovchi moddalar bilan oksidlanishi va kuchli qaytaruvchi moddalar bilan qaytarilishi mumkin. Bu reaktsiyalar issiqlik hosil qiladi. Mahsulotlarning keng assortimenti mumkin. Boshqa kislotalar singari, karboksilik kislotalar polimerizatsiya reaktsiyalarini boshlashi mumkin; boshqa kislotalar kabi, ular ko'pincha kimyoviy reaktsiyalarni katalizlaydi (tezligini oshiradi). |
| Xavf |
Teri va to'qimalarga kuchli tirnash xususiyati beruvchi. |
| Sog'liq uchun xavf |
toksik; nafas olish, yutish yoki bug'lar, changlar yoki moddalar bilan aloqa qilish (teri, ko'zlar) og'ir shikastlanish, kuyish yoki o'limga olib kelishi mumkin. Eritilgan modda bilan aloqa qilish teri va ko'zning qattiq kuyishiga olib kelishi mumkin. Suv yoki nam havo bilan reaksiya zaharli, korroziy yoki yonuvchi gazlarni chiqaradi. Suv bilan reaksiya havodagi tutun kontsentratsiyasini oshiradigan juda ko'p issiqlik hosil qilishi mumkin. Yong'in tirnash xususiyati beruvchi, korroziy va/yoki zaharli gazlarni hosil qiladi. Yong'in nazorati yoki suyultirilgan suvdan oqadigan suv korroziy va/yoki zaharli bo'lishi va ifloslanishga olib kelishi mumkin. |
| Yong'in xavfi |
Yonuvchan material: yonishi mumkin, lekin tezda yonmaydi. Modda suv bilan reaksiyaga kirishadi (ba'zilari zo'ravonlik bilan) yonuvchi, zaharli yoki korroziy gazlar va oqimlarni chiqaradi. Isitilganda bug'lar havo bilan portlovchi aralashmalar hosil qilishi mumkin: bino ichida, tashqarida va kanalizatsiya portlash xavfi. Ko'pgina bug'lar havodan og'irroqdir. Ular yer bo'ylab tarqaladi va past yoki cheklangan joylarda (kanalizatsiya, podvallar, tanklar) to'planadi. Bug'lar tutashuv manbasiga etib borishi va orqaga qaytishi mumkin. Metall bilan aloqada yonuvchi vodorod gazi paydo bo'lishi mumkin. Idishlar qizdirilganda yoki suv bilan ifloslanganda portlashi mumkin. |
| Yonuvchanlik va portlash qobiliyati |
Yonuvchan emas |
| Xavfsizlik profili |
Yutish, qorin bo'shlig'i va tomir ichiga yuborish orqali zaharlanish. Teri va shilliq pardalar uchun tirnash xususiyati beruvchi va korroziy. Mutatsiya maʼlumotlari xabar qilindi. Parchalanish uchun qizdirilganda u Br- ning zaharli bug'larini chiqaradi. Shuningdek qarang: BROMIDLAR. |
| Tozalash usullari |
Uy hayvonlari efiridan bromoasetik kislotani kristallang (b 40-60o). Uning dietil efir eritmasi alyuminiy oksidi kolonnasidan o'tkaziladi va efir xona haroratida vakuum ostida bug'lanadi. Uni izolyatsiyalangan Vigreux kolonnasi (p 11) o'rnatilgan Claisen (yog 'hammomiga botirilgan kolba) dan distillash orqali eng yaxshisi olinadi va b 108-110o/30 mm fraktsiyasi olinadi. Bu yorug'lik va namlikka sezgir. [Natelson & Gottfried Org Synth Coll Vol III 381 1955, Beilstein 2 IV 526.] LACHRYMATORY va terini tirnash xususiyati beruvchi. |